摘要:碳化硅(SiC)作為工業領域應用廣泛的一種重要非氧化物材料,可以采用甲烷(CH4)氣體,利用氧化硅的碳熱還原工藝來制備。本研究利用反作用力場(ReaxFF)分子動力學(MD)技術,采用SiO和CH4混合氣體在不同固態表面如β-SiC、石墨片、鐵、無定形SiO2等上面對反應初始階段進行觀察研究。MD結果顯示:SiO簇叢的快速形成對反應有重要影響。較高的SiO溫度增強了SiC表面單個SiC分子的形成。石墨片表面雖然也能形成SiC分子,但目前尚未發現模擬時間段內在鐵和SiO2的表面有反應發生。
關鍵詞:碳化硅, 甲烷, 反應機理
1、引言
金屬氧化物的熱碳還原是金屬加工工藝中的傳統方法,通過和還原劑(碳)的反應,該工藝可以將金屬氧化物中的氧去除掉,從而得到金屬的基本形式。還原工藝所用碳源通常為煤或焦炭,近年來甲烷逐漸替代煤和焦炭,具有碳素活度更好,還原溫度較低,能耗低、CO2排放少的優勢。
氧化還原工藝需要高溫的條件,但在高溫下會發生甲烷分解反應,生成C和H2,進而生成固態碳,和炭黑類似。為防止甲烷高溫分解,SINTEF(挪威理工大學)研究出一種特殊技術,通過SiO熱氣體和固態碳發生反應生成SiC。實驗還設計了一種特殊水冷卻噴槍,可以實現SiO熱氣體和甲烷冷氣體接觸反應以防止甲烷高溫分解成碳和氫氣。
但Si-C-H-O系統中的一些反應尚未得到明確辨認。Kai等人利用反作用力場分子動力學模擬在1600℃溫度中在β-SiC固態表面上進行SiO和CH4氣態混合物的反應;反應機理研究結果表明,SiO冷凝并聚合成環狀結構對反應機理有重要影響;而甲烷則分解為CH3、CH2或CH。CH3和SiO分解出的單個硅原子結合,最終生成SiC。實驗還研究了溫度影響因素(1200℃和1600℃)。采用不同固態表面如石墨片、鐵、無定形SiO2來分析對SiC形成的影響。
2、ADF/REAXFF模擬
ReaxFF由Duin及其同事創建,根據反作用力場方法可以進行化學反應建模,目前已納入SCM/ADF,可以進行類比和大規模MD模擬。
2.1 溫度對β-SiC表面上SiC生成的影響
利用SiC分子力場對SiO和CH4的氣態混合物反應動力學進行建模。在原子模型中,如圖1a所示,200個SiO分子和300個CH4分子隨機分散在92×92×200Å尺寸的盒子中。氣態混合物密度為0.009g/ml。盒子中間嵌入一個帶有五晶格厚度的單晶β-SiC的超晶胞。CH4氣體溫度設定為20℃,SiO氣體溫度設定為1200℃和1600℃。固定好SiC層的空間位置。MD模擬利用了Verlet和Berendsen算法速度。時間步和阻尼常數分別為0.25和500fs。
0.3ns后,每個氣態分子都被吸附到SiC層上,如圖1b所示。反應物分子數量隨時間延長而降低,如圖2所示。但SiO比CH4的消耗更快,在1.5ns后耗盡。高溫增強了CH4的分解率。值得注意的是,在0.08ns內,不同溫度對SiO還原的影響不是太大,但在0.08ns后1600℃曲線出現了陡然下降;該原因尚不明確,有待進一步研究。

圖2:1200℃和1600℃條件下CH4分子和SiO分子數目的降低
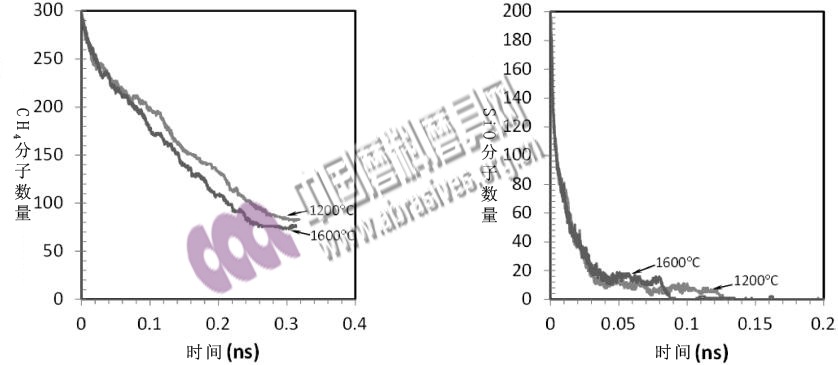
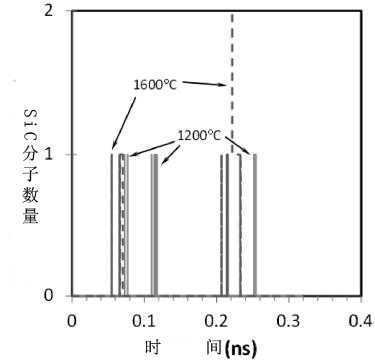
圖4:1200℃下生成的SiC快拍照

圖5a為100個SiO分子、150個CH4分子和晶格大小為5×4、4×4、3×3的3、4、5個雙層石墨片構成的建模系統。所有分子最初都隨機分散在邊長為100Å的立方體盒子中;CH4氣體溫度設定為20℃,系統的其他區域溫度設定為1600℃。其他參數設置和2.1部分相同。
0.32ns后,石墨片高度扭曲變形,但大部分反應分子都依附在上面,如圖5b所示。只有1個SiC分子是在0.311ns后形成的。這可能是由于CH和SiO直接反應的緣故(如圖6所示)。
2.3 Fe和SiO2表面上SiO和CH4的反應
如圖7a、8a所示,在Fe和SiO2表面上進行反應的兩個原子模型中,有200個SiO2分子和300個CH4分子隨機分散在92×92×200Å的立方體盒子中。盒子中間嵌入了一個帶有五晶格厚度α-鐵單晶或單個SiO2結構的超晶胞。

圖6:SiC形成過程快拍照

圖7:鐵表面上CH4+SiO反應系統在1400℃下的初始結構(a)和最終結構(b)

圖8:SiO2表面上CH4+SiO反應系統在1600℃下的初始結構(a)和最終結構(b)

在較長一段時間(0.5ns)之后,盡管大部分氣態分子都依附在了固態表面,但沒有SiC生成,如圖7b和8b所示。
3、結論
本研究利用反作用力場(ReaxFF)分子動力學(MD)技術,采用SiO和CH4混合氣體在不同固態表面如β-SiC、石墨片、鐵、無定形SiO2等上面對SiC形成機理進行研究。實驗結果顯示,SiO簇叢的快速形成對反應有著重要影響。SiO氣體的高溫增強了SiC表面上單個SiC分子的形成。石墨片表面雖然也能形成SiC分子,但目前尚未發現模擬時間段內在鐵和SiO2的表面有反應發生。
Methane, Chem. Eng. Technol 30(8): 1123–1128.
2. Jamshidi, E. & Ebrahim, H.A. 2008. A new clean process for barium carbonate preparation by barite reduction with methane, Chem Eng Process 47(9): 567–1577.
3. Khoshandam, B., Kumar, R.V. & Jamshidi, E. 2006. Producing Chromium Carbide Using Reduction of Chromium Oxide with Methane, AIChE Journal 52(3): 1094–1102.
4. Monsen, B., Kolbeinsen, L., Prytz, S., Myrvågnes, V. & Tang, K. 2013. Possible Use of Natural Gas For Silicon or ferrosilicon Production, in Proceeding of the 13th International Ferroalloys Congress, Kazakhstan, Vol. 1: 467–478.
5. Newsome, D., Sengupta, D., Foroutan, H., Russo, M.F. & van Duin, A.C.T. 2012. Oxidation of Silicon Carbide by O2 and H2O: A ReaxFF Reactive Molecular Dynamics Study: Part I, J. Phys. Chem. C 116(30): 16111–16121.
6. Ostrovski, O. & Zhang, G. 2006. Reduction and Carburization of Metal Oxides by Methane-Containing Gas, AIChE Journal 52(1): 300–310.
7. Ostrovski, O., Zhang, G., Kononov, R., Dewan, M.A.R. & Li, J. 2010. Carbothermal Solid State
Reduction of Stable Metal Oxides, Steel Research Int. 81(10): 841–846.
8. SCM 2014. ReaxFF 2014, Vrije Universiteit, Amsterdam, The Netherlands, http://www.scm.com.
9. Tang, K., Ma, X., Andersson, S. & Dalaker, H. 2015. Kinetics between SiO and CH4 at High Temperature. In Jiang, T. etc. (eds), 6th International Symposium on High-Temperature Metallurgical Processing: 349–356, TMS (The Minerals, Metals & Materials Society). van Duin, A.C.T. 2002. ReaxFF User Manual.


 手機資訊
手機資訊 官方微信
官方微信







 豫公網安備41019702003604號
豫公網安備41019702003604號